Angeborene Immundefekte sind eine heterogene Krankheitsgruppe mit über 550 bekannten monogenetischen Entitäten. Sie manifestieren sich oftmals im Kindesalter; auch genuine adulte Erstmanifestationen sind nicht selten. Die klassischen „10 Warnzeichen“ wurden in den 1990er-Jahren entwickelt und bilden das heutige Krankheitsspektrum der IEI nur unvollständig ab: Autoimmunität, Dysregulation oder laborchemische Auffälligkeiten bleiben dabei häufig unberücksichtigt. Wird die Diagnose zu spät gestellt, haben bis zu 50 % der Patienten bereits dauerhafte Organschäden erlitten.Skalierbare, auf künstlicher Intelligenz und elektronischen Patientendaten basierende Screeningstrategien, bei denen Algorithmen automatisiert klinische Muster erkennen und Risikopersonen identifizieren, können das Neugeborenen-Screening ergänzen und eine frühere Diagnosestellung auch jenseits des Säuglingsalters ermöglichen. Die molekulargenetische Diagnose ist Grundlage der personalisierten Therapie: Sie ermöglicht gezielte Immunglobulinsubstitution, antimikrobielle Prophylaxe, gezielte Therapien sowie kurative Ansätze wie hämatopoetische Stammzelltransplantation und Gentherapie. Die Frühdiagnose ist damit heute entscheidend für eine prognoseverbessernde Behandlung.
Kostenlose, evidenzbasierte CME-Fortbildungen für Hämatologen. Vertiefen Sie Ihre Expertise zum Multiplen Myelom, Leukämien, Lymphomen, Anämien, Gerinnungsstörungen oder CAR-T-Zell-Therapien. Nutzen Sie praxisnahe Kurse und sichern sich schnell und bequem CME-Punkte.





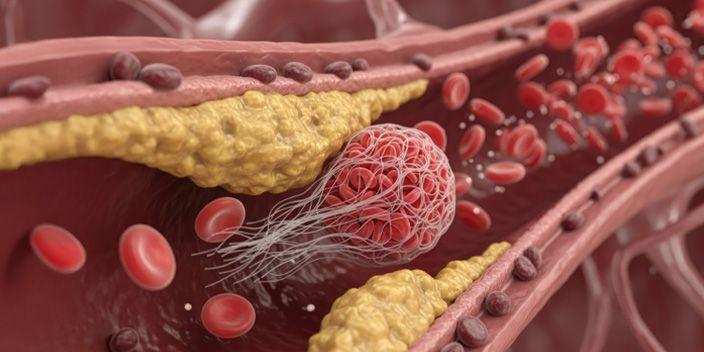
Thrombotische Mikroangiopathie nach Stammzelltransplantation
Die allogene hämatopoetische Stammzelltransplantation (allo-HSZT) ist eine hochwirksame, aber toxische Therapie, die bei aggressiven Leukämien und anderen hämatologischen Erkrankungen eingesetzt wird. Trotz verbesserter Konditionierung und Supportivtherapie liegt die transplantationsbedingte Mortalität weiter bei ca. 10 %. Eine intensivmedizinische Behandlung ist häufig erforderlich. Die Prognose hat sich in den letzten Jahren jedoch deutlich verbessert.Eine gefürchtete Komplikation der allo-HSZT ist die transplantationsassoziierte thrombotische Mikroangiopathie (TA-TMA), die bei Erwachsenen in ca. 10 % der Fälle auftritt. Sie ist durch Endothelschädigung, Komplementaktivierung und oftmals Überlappung mit schwerer Graft-versus-Host-Reaktion gekennzeichnet. Diagnostisch wegweisend sind Schistozyten, ein Lactatdehydrogenase-Anstieg, transfusionsrefraktäre Thrombozytopenie, Hypertonie und Proteinurie. Differenzialdiagnostisch muss TA-TMA v. a. von Sepsis und disseminierter intravasaler Koagulopathie abgegrenzt werden. Früherkennung und eine umfassende interdisziplinäre Behandlung sind entscheidend für die Prognose. Hierbei stehen allgemeine intensivmedizinische Maßnahmen im Vordergrund. Eine Plasmapherese hat bei TA-TMA kaum Nutzen. Komplementinhibitoren (v. a. Eculizumab, off Label) zeigen in Fallserien und Studien vielversprechende Ergebnisse.
Am Ende dieser Fortbildung kennen Sie...

Neue Therapieansätze bei triple-class refraktärem Multiplen Myelom
Der Schwerpunkt dieser Fortbildung liegt auf den Behandlungsmöglichkeiten für Patienten mit fortgeschrittenem Multiplen Myelom (MM), die bereits eine Triple-Class-Refraktärität gegenüber den verfügbaren Therapieoptionen aufweisen. Die Bezeichnung Triple-Class-refraktär bezieht sich auf Patienten, die bereits mit einem Proteasom-Inhibitor, einem Immunmodulator und einem Anti-CD-38-Antikörper behandelt wurden und die während der Behandlung oder innerhalb von 60 Tagen nach Abschluss der Therapie einen Krankheitsprogress erfahren haben. Neben den Therapieoptionen, die bereits in den europäischen Leitlinien von 2021 und der Deutschen S3-Leitlinie „Diagnostik, Therapie und Nachsorge für Patienten mit monoklonaler Gammopathie unklarer Signifikanz (MGUS) oder Multiplem Myelom“ von 2022 empfohlen werden, werden auch neuere zugelassene Substanzen vorgestellt. Dies schließt insbesondere Melphalanflufenamid, das auch unter dem Namen Melflufen bekannt und seit August 2022 zur Behandlung des Triple-Class-refraktären MM zugelassen ist, ein. Melflufen ist ein Vertreter der neuen Wirkstoffklasse der Peptid-Drug-Konjugate (PDC), der für die Behandlung des fortgeschrittenen MM zugelassen wurde. Es handelt sich um eine vielversprechende Therapieoption, die sich durch eine Kombination aus guter klinischer Wirksamkeit, einem gut beherrschbaren Nebenwirkungsprofil und der Erhaltung der Lebensqualität auszeichnet.
Am Ende dieser Fortbildung kennen Sie...

Die nicht schwere Hämophilie A
Während Behandlung und Management der schweren Hämophilie gut etabliert sind, gibt es weit weniger Informationen zur nicht schweren Hämophilie. Aufgrund der großen Variabilität in der Symptomausprägung werden diese Patienten häufig nicht in klinische Studien oder Studien zur Lebensqualität einbezogen. Da diese Patienten tendenziell weniger häufig blutungsbedingte Symptome haben, können sie nicht immer eine Gelenkblutung direkt erkennen. Darüber hinaus ist es möglich, dass auch Ärzte, die nicht auf Hämophilie spezialisiert sind, bei Patienten mit leichter bis moderater Hämophilie Gelenkprobleme nicht so schnell mit Blutungen in Verbindung bringen. Die nicht schwere Hämophilie wird daher meist später erkannt, was eine adäquate Behandlung verzögert und letztlich zu Gelenk- oder anderen Gewebeschäden führen kann. Trotz ihres milderen Blutungsphänotyps kann die Behandlung von Patienten mit nicht schwerer Hämophilie A eine Herausforderung darstellen, da die meisten Behandlungsentscheidungen weitgehend aus den Daten der schweren Hämophilie A abgeleitet werden müssen. Diese Fortbildung soll dazu beitragen, die Versorgung von Patienten mit nicht schwerer Hämophilie zu verbessern, indem neuere Studienergebnisse vorgestellt und praktische Handlungsempfehlungen gegeben werden.
Am Ende dieser Fortbildung kennen Sie...

Hämophilie A in der Adoleszenz
Im Deutschen Hämophilieregister ist etwa jeder vierte dort registrierte Hämophilie-A-Patient unter 18 Jahre alt. Bis zum 18. Lebensjahr werden die Betroffenen in der Regel von Kinder- und Jugendärzten betreut. Mit dem Eintritt ins Erwachsenenalter erfolgt meist die Transition, was für Patienten und Behandler herausfordernd sein kann. In dieser Fortbildung werden die Hürden und die Erfolgsfaktoren für eine gelungene Transition näher beleuchtet. Sie erfahren u. a., wie es um die Adhärenz mit der prophylaktischen Behandlung der Hämophilie bei adoleszenten Patienten bestellt ist. Außerdem betrachten wir die möglichen Folgen eines Wechsels von der Prophylaxe zur On-Demand-Behandlung und gehen der Frage nach dem besten Zeitpunkt für den Beginn der Prophylaxe nach.
Am Ende dieser Fortbildung kennen Sie...

Komorbiditäten bei Hämophilie A
Die Zahl von Patienten mit schwerer Hämophilie über 60 Jahre hat über die letzten Jahrzehnte stark zugenommen. Zusätzlich zu den üblichen Alterserkrankungen können bei Hämophilie-Patienten spezifische Probleme auftreten. In dieser Fortbildung werden die häufigsten Komorbiditäten älterer Hämophilie-Patienten besprochen. Sie erfahren u. a., was es bei antithrombotischen Therapien zur Behandlung von Vorhofflimmern zu beachten gilt und warum Hypertonie für Hämophilie-Patienten ein besonders gefährlicher Risikofaktor sein kann. Wir listen auf, welche Medikamente zur Schmerzbehandlung bei Hämophilie geeignet sind und welche nicht. Auch wird die Hämaturie als bekannte Begleiterscheinung der Hämophilie A näher beleuchtet.
Am Ende dieser Fortbildung kennen Sie...
Hämophilie A heute – eine individualisierte Therapie
Die Behandlung der Hämophilie A basiert auf der Substitution des fehlenden Gerinnungsfaktors VIII (FVIII), die bei Bedarf oder prophylaktisch erfolgen kann. In den im Jahr 2020 aktualisierten nationalen und internationalen Leitlinien wird für Patienten mit schwerer Hämophilie A und für einige Patienten mit mittelschwerer Hämophilie A die dauerhafte Prophylaxe empfohlen. Die Bedarfstherapie stellt aufgrund des fehlenden Gelenkschutzes und der hohen annualisierten Blutungsraten keine langfristige Behandlungsoption mehr dar. Um die, für die Dauerbehandlung, erforderlichen FVIII-Talspiegel 3 bis 5 % zu erreichen, wurden rekombinante Extended-Half-Life-FVIII-Produkte (EHL-rFVIII) entwickelt. Diese können sich signifikant in ihrer Pharmakokinetik (PK) unterscheiden, wie Head-to-Head-Studien zeigen. In dieser Fortbildung erfahren Sie u. a., welche Langzeitergebnisse EHL-rFVIII-Produkte in Studien erzielt haben. Außerdem erhalten Sie Einblick in die Herausforderungen der FVIII-Dosierung im Rahmen einer personalisierten Prophylaxe. Sie lernen die Möglichkeiten der PK-adjustierten Prophylaxe sowie die Vorteile der digitalen Dokumentation mithilfe von Smartphone-Apps kennen.
Am Ende dieser Fortbildung kennen Sie...

Diagnostik und Behandlung der Synovitis bei Hämophilie A
Unter blutungsbedingten Entzündungen der Synovia leiden viele Hämophiliepatienten. Nehmen Synovitiden einen chronischen Verlauf, können irreversible Gelenkschäden die Folge sein. In dieser Fortbildung wird die Pathophysiologie näher erläutert, die dem Teufelskreis aus Gelenkeinblutungen, Bewegungseinschränkungen und Entzündungen zugrunde liegt. Sie erhalten praktische Hinweise für die Diagnostik und Behandlung der hämophilen Synovitis. Erfahren Sie außerdem, wie sich die Umstellung von einem Faktor-VIII-Produkt mit Standardhalbwertszeit (SHL) auf ein Produkt mit verlängerter Halbwertszeit („extended half-life“, EHL) auf die Gelenkeinblutungsrate auswirken kann.
Am Ende dieser Fortbildung kennen Sie...
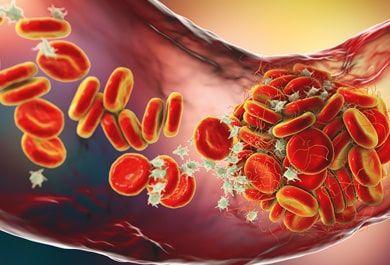
Update: Herausforderung Antikoagulation bei nv VHF, Diabetes und Niereninsuffizienz
Patienten mit nicht valvulärem Vorhofflimmern (nv VHF) sollten je nach erreichter Punktzahl im CHA2DS2-VASc-Score eine Antikoagulation erhalten. Häufig bestehen jedoch neben dem nv VHF weitere Komorbiditäten, wie eine chronische Niereninsuffizienz (CKD) oder ein Diabetes mellitus, die das Schlaganfall- und Mortalitätsrisiko erhöhen. Unter diesen Umständen die geeignete Antikoagulation einzuleiten und anzupassen, stellt in der Praxis oft eine Herausforderung dar. Bei Patienten mit nv VHF und CKD empfehlen die ESC-Leitlinien neue orale Antikoagulanzien (NOAK) zur Schlaganfallprophylaxe, da diese in Studien mit einem geringeren Risiko für eine Verschlechterung der Nierenfunktion assoziiert waren als Vitamin-K-Antagonisten (VKA). Bei der Auswahl eines NOAK sind unbedingt die Kriterien für eine Dosisreduktion zu beachten, zum Beispiel Alter, Gewicht und Komedikation. Die nicht bestimmungsgemäße Dosisreduktion kann bei nv VHF-Patienten das Schlaganfallrisiko erhöhen.
Am Ende dieser Fortbildung kennen Sie...
Hemmkörper bei Hämophilie A und B
Die Bildung von Hemmkörpern gehört zu den gefürchteten Komplikationen der Hämophilie- behandlung. Spezifische neutralisierende IgG-Antikörper richten sich gegen das substituierte Faktorprodukt und hemmen gezielt die prokoagulatorische Wirkung des Gerinnungsfaktors. Die Patienten neigen zu stärkeren und vor allem spontanen Blutungen, die lebensbedrohlich sein können. Insbesondere bei schwerer Hämophilie A kommt es bei etwa 25 bis 40 % der Patienten zur Entstehung von Hemmkörpern, bei der schweren Hämophilie B deutlich seltener. Es ist entscheidend, Hemmkörper frühzeitig zu erkennen, um eine adäquate Behandlung einzuleiten. In vielen Fällen werden diese durch ein routinemäßiges Hemmkörper-Screening nach den ersten Faktorexpositionen festgestellt. In Abhängigkeit von der Höhe der gemessenen Hemmkörperkonzentration, auch Hemmkörpertiter genannt, stehen verschiedene Therapieoptionen zur Verfügung. Das primäre Ziel der Behandlung ist die dauerhafte Beseitigung des Hemmkörpers durch eine Immuntoleranzinduktion. In dieser Fortbildung werden neben den pathophysiologischen Mechanismen der Hemmkörperbildung ausführlich die Risikofaktoren für deren Entstehung besprochen. Sie erfahren, mit welchen Tests Hemmkörper festgestellt und quantifiziert werden können. Wir stellen Ihnen die verschiedenen Medikamente vor, die aktuell zur Behandlung von Hemmkörpern zur Verfügung stehen, und erläutern die Vorgehensweise bei der Immuntoleranzinduktion. Schließlich gehen wir auf die Bedeutung der Zusammenarbeit aller an der Versorgung des Hämophiliepatienten beteiligten Personen ein.
Am Ende dieser Fortbildung kennen Sie...

Der ältere Hämophiliepatient
Dank zunehmend besserer Behandlungsmöglichkeiten haben Menschen mit Hämophilie eine hohe Lebenserwartung, die fast der der Allgemeinbevölkerung entspricht. Allerdings leiden viele Hämophilie-Patienten im Alter häufiger an orthopädischen Problemen bis hin zur Invalidität. Auch kommen chronische Infektionskrankheiten wie HIV, Hepatitis B und C (HBV, HCV) auf Grund der in den 80er Jahren aufgetretenen Verunreinigungen von plasmatischen Faktorkonzentraten oder Blutplasma mit entsprechenden Spätfolgen häufiger vor. Obwohl eine prophylaktische Substitution von Gerinnungsfaktoren Vorteile gegenüber der Bedarfsbehandlung bringt, wenden bisher nicht alle älteren Patienten eine regelmäßige Prophylaxe an. In dieser Fortbildung werden ausführlich die häufigsten Komorbiditäten bei älteren Hämophilie-Patienten besprochen. Sie erfahren, wie dem erhöhten Sturzrisiko zu begegnen und was bei einer Schmerztherapie zu berücksichtigen ist. Wir erklären, welche Maßnahmen vor und während invasiver Eingriffe oder bei Vorsorgemaßnahmen wie Gastroskopie oder Rektoskopie erforderlich sind. Auch psychosoziale Aspekte und der Einfluss auf die Lebensqualität werden beleuchtet. Schließlich gehen wir auf die Bedeutung der Zusammenarbeit aller an der Versorgung des Hämophilie-Patienten Beteiligten ein.